- Apotheken-Notdienst
-
Podcast: "gecheckt!"
- Podcasts: Allergien
- Podcasts: Apotheke
- Podcasts: Arzneimittel
- Podcasts: Baby und Familie
- Podcasts: Diabetes
- Podcasts: Erkältung
- Podcasts: Ernährung
- Podcasts: Frauengesundheit
- Podcasts: Gesund leben
- Podcasts: Haut & Haare
- Podcasts: Magen-Darm
- Podcasts: Männergesundheit
- Podcasts: Medizin
- Podcasts: Naturheilkunde
- Podcasts: Psychologie
- Podcasts: Sport & Bewegung
- Podcasts: Zähne
- Podcast: Was ist das überhaupt?
- Newsletter
- Apotheke
- Medizin
- Naturheilkunde
- Ernährung
- Sport & Wellness
- Jung & Alt
- Frau & Mann
- Gesellschaft
- Service
- Gewinnspiel
- Das Apotheken Magazin
Baby & FamilieSeniorenGesundheit
Neue Verordnung erhöht Sicherheit für Patienten mit Implantaten
Eine neue Verordnung über die Abgabe von Medizinprodukten soll für mehr Sicherheit für Patienten sorgen, die mit künstlichen Gelenken oder Brustimplantaten versorgt werden. Darauf weist das Bundesministerium für Gesundheit hin.
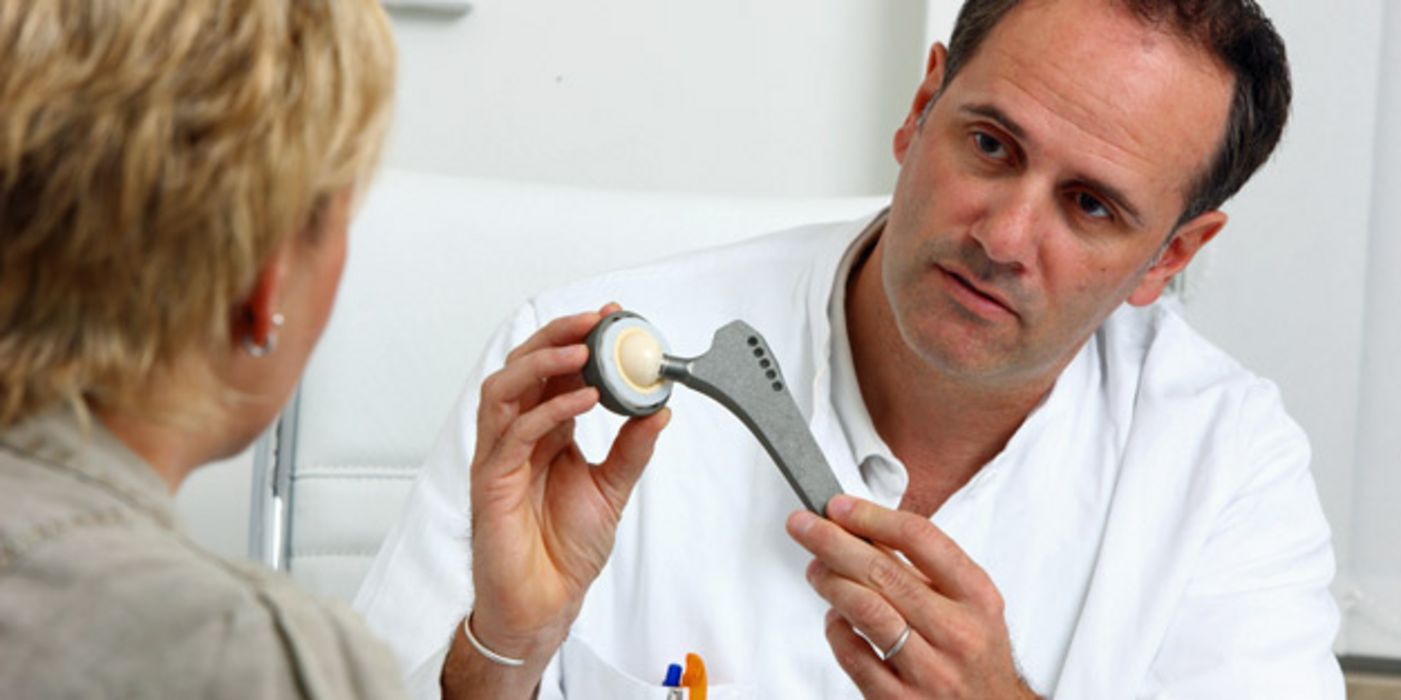
© AOK-Mediendienst
Künftig erhalten alle Patienten, denen z.B. Herzklappen, Hüft- oder Kniegelenke oder auch Brustimplantate eingesetzt werden,
- eine Patienteninformation, die die für die Sicherheit des Patienten notwendigen Verhaltensanweisungen enthält und
- einen Implantatepass, der u.a. die Bezeichnung, Art und Typ sowie die Seriennummer des Implantats enthält. Dadurch wird ein zweites Sicherheitselement geschaffen, damit die Patienten etwa bei entsprechenden öffentlichen Warnungen selbst kontrollieren können, ob ihr Implantat betroffen ist.
Zusätzlich müssen die Gesundheitseinrichtungen, in denen die Implantate eingesetzt werden, eine geeignete Dokumentation anlegen. Diese soll gewährleisten, dass die betroffenen Patienten z.B. im Falle von Rückrufen von Produkten innerhalb von drei Werktagen ermittelt werden können.
Bis zum 1. Oktober 2015 haben Hersteller und Gesundheitseinrichtungen jetzt Zeit, die technischen Voraussetzungen für die Einführung dieser drei Punkte zu schaffen. Wie relevant diese Anforderungen sind, zeigte sich z.B. bei dem Rückruf von minderwertigen Brustimplantaten in Frankreich im Jahr 2011, der mehrere Zehntausend Frauen betraf und auch in Deutschland für Unsicherheit sorgte.
BMG/RF
Medikamente ohne Zuzahlung
Alle zwei Wochen neu: die aktuelle Liste der zuzahlungsfreien Arzneimittel.
Anzeige
Besuchen Sie am 26.04. in Marburg den MPN Patient*innentag für Betroffene und Angehörige…
Arzneimitteldatenbank
Medikamenten-Name oder Wirkstoff eingeben für mehr Informationen.
Podcast "gecheckt!"
Die körpereigenen Botenstoffe beeinflussen uns tiefgreifend auf vielen Ebenen und in fast allen…
Aktuelle Nachrichten
aus Apotheke, Forschung und Gesundheitspolitik.
Krankheiten von A - Z
In diesem Lexikon finden Sie umfassende Beschreibungen von etwa 400 Krankheitsbildern

